氢氧化锂
氢氧化锂(分子式:LiOH)是锂的氢氧化物,具腐蚀性,室温下为白色潮解性晶体。易溶于水,溶液呈强碱性,微溶于乙醇,存在无水和一水合物两种状态。
| 氢氧化锂 | |
|---|---|
 | |
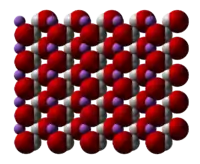 | |
| IUPAC名 Lithium hydroxide | |
| 识别 | |
| CAS号 | 1310-66-3((monohydrate)) 1310-65-2 |
| ChemSpider | 3802 |
| InChI |
|
| InChIKey | WMFOQBRAJBCJND-REWHXWOFAT |
| Gmelin | 68415 |
| UN编号 | 2680 |
| ChEBI | 33979 |
| RTECS | OJ6307070 |
| 性质 | |
| 化学式 | LiOH |
| 摩尔质量 | 23.95 g·mol⁻¹ |
| 外观 | 白色潮解固体 |
| 密度 | 1.46 g/cm3 (固) |
| 熔点 | 462 °C |
| 沸点 | 924 °C(分解) |
| pKb | 0.18 (LiOH(aq) = Li+ + OH–) [1] |
| 危险性 | |
| 主要危害 | 腐蚀性 |
| 闪点 | 不可燃 |
| 相关物质 | |
| 其他阴离子 | 氧化锂 |
| 其他阳离子 | 氫氧化鈉 氫氧化鉀 氫氧化銣 氫氧化銫 氫氧化鍅 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
生产
- 2 Li + 2 H2O → 2 LiOH + H2
- Li2O + H2O → 2 LiOH
- Li2CO3 + Ca(OH)2 → 2LiOH + CaCO3
反应
氢氧化锂是空间飞船、潜艇和水下呼吸器中呼吸气体净化系统中所用的材料,可以吸收呼出气中的二氧化碳。其相对分子质量小,相对其他净气物质效率更高,1克的无水氢氧化锂可以吸收450cm3的二氧化碳气体。该过程中涉及的反应有:
- 2 LiOH·H2O + CO2 → Li2CO3 + 3 H2O
- 2 LiOH + CO2 → Li2CO3 + H2O
一水合氢氧化锂在100-110 °C失去结晶水。
- LiOH·H2O → LiOH + H2O
参见
参考资料
- Greenwood, N. N.; Earnshaw, A. 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.